Общая характеристика неметаллов 2 вариант. Неметаллы. Общая характеристика. Строение атома. Физические свойства. Положение неметаллов в ПС
ХИМИЧЕСКИЕ СВОЙСТВА ВОДОРОДА
1. С МЕТАЛЛАМИ
(Li, Na, К, Rb, Cs, Са, Sr, Ва) → с щелочными и щелочноземельными металлами при нагревании образует твёрдые нестойкие вещества гидриды, остальные металлы не реагируют.
2K + H₂ = 2KH (гидрид калия)
Ca + H₂ = CaH₂
2. С НЕМЕТАЛЛАМИ
с кислородом, галогенами при нормальных условиях, при нагревании реагирует с фосфором, кремнием и углеродом, с азотом при наличии давления и катализатора.
2Н₂ + O₂ = 2Н₂O Н₂ + Cl₂ = 2HCl
3Н₂ + N₂↔ 2NH₃ H ₂ + S = H₂S
3. ВЗАИМОДЕЙСТВИЕ С ВОДОЙ
С водой не реагирует
4.ВЗАИМОДЕЙСТВИЕ С ОКСИДАМИ
Восстановливает оксиды металлов (неактивных) и неметаллов до простых веществ:
CuO + H₂ = Cu + H₂O 2NO + 2H₂ = N₂ + 2H₂O
SiO₂ + H₂ = Si + H₂O
5.ВЗАИМОДЕЙСТВИЕ С КИСЛОТАМИ
С кислотами не реагирует
6.ВЗАИМОДЕЙСТВИЕ С ЩЕЛОЧАМИ
С щелочами не реагирует
7.ВЗАИМОДЕЙСТВИЕ С СОЛЯМИ
Восстанавливает малоактивные металлы из солей
CuCl₂ + H₂ = Cu + 2HCl
ХИМИЧЕСКИЕ СВОЙСТВА КИСЛОРОДА
1.ВЗАИМОДЕЙСТВИЕ С МЕТАЛЛАМИ
С щелочными металлами при нормальных условиях – оксиды и пероксиды (литий – оксид, натрий – пероксид, калий, цезий, рубидий – надпероксид
4Li + O2 = 2Li2O (оксид)
2Na + O2 = Na2O2 (пероксид)
K+O2=KO2 (надпероксид)
С остальными металлами главных подрупп при нормальных условиях образует оксиды со степенью окисления, равной номеру группы
2 С a+O2=2 С aO
4Al + O2 = 2Al2O3
1.ВЗАИМОДЕЙСТВИЕ С МЕТАЛЛАМИ
С металлами побочных подгрупп образует при нормальных условиях и при нагревании оксиды разной степени окисления, а с железом железную окалину Fe 3 O 4 ( FeO ∙ Fe 2 O 3)
3Fe + 2O2 = Fe3O4 4Cu + O₂ = 2Cu₂⁺¹O (красный);
2Cu + O₂ = 2Cu⁺²O (чѐрный); 2Zn + O₂ = ZnO
4Cr + 3О2 = 2Cr2⁺³О3
образует оксиды – часто промежуточной степени окисления
C + O ₂(изб)= CO ₂; C + O ₂ (нед) = CO
S + O₂ = SO₂ N₂ + O₂ = 2NO - Q
3.ВЗАИМОДЕЙСТВИЕ С ВОДОЙ
С водой не реагирует
4.ВЗАИМОДЕЙСТВИЕ С ОКСИДАМИ
Окисляет низшие оксиды до оксидов с более высокой степенью окисления
Fe⁺²O + O2 = Fe2⁺³O3; C⁺²O + O2 = C⁺⁴O2
5.ВЗАИМОДЕЙСТВИЕ С КИСЛОТАМИ
Безводные бескислородные кислоты (бинарные соединения) сгорают в атмосфере кислорода
2H2S + O2 = 2S + 2H2O 2H2S + 3O2 = 2SO2 + 2H2O
В кислородсодержащих повышает степень окисления неметалла.
2HN⁺³O2 + O2 = 2HN⁺⁵O3
6.ВЗАИМОДЕЙСТВИЕ С ОСНОВАНИЯМИ
Окисляет неустойчивые гидроксиды в водных растворах до более высокой степени окисления
4Fe(OH)2 + O2 + 2H2O = 4Fe(OH)3
7.ВЗАИМОДЕЙСТВИЕ С СОЛЯМИ И БИНАРНЫМИ СОЕДИНЕНИЯМИ
Вступает в реакции горения.
4FeS2 +11O2 = 2Fe2O3 + 8SO2
CH4 + 2O2 = CO2 + 2H2O
4NH3 + 3O2 = 2N2 + 6H2O
Каталитическое окисление
NH3 + O2 = NO + H2O
ХИМИЧЕСКИЕ СВОЙСТВА ГАЛОГЕНОВ
1.ВЗАИМОДЕЙСТВИЕ С МЕТАЛЛАМИ
С щелочными при нормальных условиях, с F , Cl , Br воспламеняются:
2 Na + Cl 2 = 2 NaCl (хлорид)
Щелочноземельные и алюминий реагируют при нормальных условиях:
С a+Cl2= С aCl2 2Al+3Cl2 = 2AlCl3
Металлы побочных подгрупп при повышенных температурах
Cu + Cl₂ = Cu⁺²Cl₂
2Cu + I₂ = 2Cu⁺¹I (не бывает йодида меди (II)!)
2Fe + ЗС12 = 2Fe⁺³Cl3 хлорид железа (III)
Фтор реагирует с металлами (часто со взрывом), включая золото и платину.
2Au + 3F₂ = 2AuF
2.ВЗАИМОДЕЙСТВИЕ С НЕМЕТАЛЛАМИ
С кислородом непосредственно не взаимодействуют(исключение F₂) , реагируют с серой, фосфором, кремнием. Химическая активность у брома и йода выражена слабее, чем у фтора и хлора:
Н2 + F 2 = 2Н F ; Si + 2 F 2 = SiF 4.; 2 P + 3 Cl 2 = 2 P ⁺³ Cl 3; 2 P + 5 Cl 2 = 2 P ⁺⁵ Cl 5; S + 3 F 2 = S ⁺⁶ F 6;
S + Cl2 = S⁺²Cl2
F ₂
Реагирует с кислородом: F 2 + O 2 = O ⁺² F 2
Реагирует с другими галогенами: Cl ₂ + F ₂ = 2 Cl ⁺¹ F ¯¹
Реагирует даже с инертными газами 2 F ₂ + Xe = Xe ⁺⁸ F ₄¯¹.
3.ВЗАИМОДЕЙСТВИЕ С ВОДОЙ
Фтор при нормальных условиях образует плавиковую кислоту + + О₂
2F2 + 2H2O → 4НF + О2
Хлор при повышении температуры образует хлороводородную кислоту + О₂,
2Сl₂ + 2H₂O → 4HCl + O₂
при н.у. - «хлорная вода»
Сl2 + Н2О ↔ НСl + НСlO (хлороводородная и хлорноватистая кислоты)
Бром при нормальных условиях образует «бромную воду»
Br2 + Н2О ↔ НBr + HBrО (бромоводородная и бромноватистая кислоты
Йод →реакция не идет
I2 + H₂O ≠
5.ВЗАИМОДЕЙСТВИЕ С ОКСИДАМИ
РЕАГИРУЕТ только фтор F₂ , вытесняя кислород из оксида, образуя фториды
SiO2‾² + 2F2⁰ = SiF4‾¹ + O2⁰
6.ВЗАИМОДЕЙСТВИЕ С КИСЛОТАМИ.
реагируют с бескислородными кислотами, вытесняя менее активные неметаллы.
H2S‾² + I2⁰ → S⁰↓+ 2HI‾
7.ВЗАИМОДЕЙСТВИЕ С ЩЕЛОЧАМИ
ФТОР образует фторид + кислород и воду
2F2 + 4NaOH = 4NaF¯¹ + O2 + 2H2O
ХЛОР при нагревании образует хлорид, хлорат и воду
3 Cl ₂ + 6 KOH = 5 KCl ¯¹ + KCl ⁺⁵ O 3 + 3 H 2 O
На холоде хлорид, гипохлорат и воду, с гидроксидом кальция хлорную известь и воду
Cl2 + 2KOH-(холод)= KCl¯¹ + KCl⁺¹O + H2O
Cl2 + Ca(OH) 2 = CaOCl2(хлорная известь– смесь хлорида, гипохлорита и гидроксида) + H2O
Бром при нагревании → бромид, бромат и и воду
3Br2 + 6KOH =5KBr¯¹ + KBr ⁺⁵O3 + 3H2O
Йод при нагревании → иодид, иодат и воду
3I2 + 6NaOH = 5NaI¯¹ + NaI ⁺⁵O3 + 3H2O
9.ВЗАИМОДЕЙСТВИЕ С СОЛЯМИ
Вытеснение менее активные галогены из солей
2KBr + Cl2 → 2KCl + Br2
2KCl + Br2 ≠
2KCl + F2→ 2KF + Cl2
2KBr + J2≠
Окисляют в солях неметаллы до более высокой степени окисления
2Fe⁺²Cl2 + Cl2⁰ → 2Fe⁺³Cl 3 ‾¹
Na2S⁺⁴O3 + Br2⁰ + 2H2O →Na2S⁺⁶O4 + 2HBr‾
ХИМИЧЕСКИЕ СВОЙСТВА СЕРЫ
1.ВЗАИМОДЕЙСТВИЕ С МЕТАЛЛАМИреагирует при нагревании даже с щелочными металлами, с ртутью при нормальных условиях: с серой – сульфиды:
2K + S = K2S
2Cr + 3S = Cr2⁺³S3 Fe + S = Fe⁺²S
2.ВЗАИМОДЕЙСТВИЕ С НЕМЕТАЛЛАМИ
При нагревании с водородом, c кислородом (сернистый газ) c галогенами (кроме йода), с углеродом, азотом и кремнием и не реагирует
S + Cl₂ = S⁺²Cl₂ ; S + O₂ =S⁺⁴O₂
H₂ + S = H₂S¯² ; 2P + 3S = P₂S₃¯²
С + 3S = CS₂¯²
С ВОДОЙ, ОКСИДАМИ, СОЛЯМИ
НЕ РЕАГИРУЕТ
3.ВЗАИМОДЕЙСТВИЕ С КИСЛОТАМИ
Окисляется серной кислотой при нагревании до сернистого газа и воды
2H2SO4 ( конц ) = 2H2O + 3S⁺⁴O2
Азотной кислотой при нагревании до серной кислоты, оксида азота (+4) и воды
S + 6HNO3( конц ) =H2SO4 + 6N⁺⁴O2 + 2H2O
4.ВЗАИМОДЕЙСТВИЕ С ЩЕЛОЧАМИ
При нагревании образует сульфит, сульфид + вода
3S + 6KOH = K2SO3 + 2K2S + 3H2O
ХИМИЧЕСКИЕ СВОЙСТВА АЗОТА
1.ВЗАИМОДЕЙСТВИЕ С МЕТАЛЛАМИреакции протекают при нагревании (исключение: литий с азотом при нормальных условиях) :
С азотом – нитриды
6Li + N2 = 3Li2N (нитрид лития) (н.у.) 3Mg + N2 =Mg3N2 (нитрид магния) 2Cr + N2 = 2CrN
У железа в данных соединениях степень окисления +2
2.ВЗАИМОДЕЙСТВИЕ С НЕМЕТАЛЛАМИ
(из-за тройной связи азот очень малоактивен). При обычных условиях с кислородом не реагирует. Реагирует с кислородом только при высокой температуре (электрическая дуга), в природе – во время грозы
N2+O2=2NO ( эл . дуга , 3000 0C)
С водородом при высоком давлении, повышенной температуре и в присутствии катализатора:
t,p,kat
3N2+3H2 ↔ 2NH3
С ВОДОЙ, ОКСИДАМИ, КИСЛОТАМИ, ЩЕЛОЧАМИ И СОЛЯМИ
НЕ РЕАГИРУЕТ
ХИМИЧЕСКИЕ СВОЙСТВА ФОСФОРА
1.ВЗАИМОДЕЙСТВИЕ С МЕТАЛЛАМИ
реакции протекают при нагревании с фосфором – фосфиды
3Ca + 2P =K3P2, У железа в данных соединениях степень окисления +2
2.ВЗАИМОДЕЙСТВИЕ С НЕМЕТАЛЛАМИ
Горение в кислороде
4P + 5O₂ = 2P₂⁺⁵O₅ 4P + 3O₂ = 2P₂⁺³O₃
С галогенами и серой при нагревании
2P + 3Cl₂ = 2P⁺³Cl₃ 2P + 5Cl₂ = 2P⁺⁵Cl₅; 2P + 5S = P₂⁺⁵S₅
С водородом, углеродом, кремнием непосредственно не взаимодействует
С ВОДОЙ И ОКСИДАМИ
НЕ РЕАГИРУЕТ
3.ВЗАИМОДЕЙСТВИЕ С КИСЛОТАМИ
С концентрированной азотной кислотой оксид азота (+4), с разбавленной оксид азота (+2) и фосфорная кислота
3P + 5HNO₃(конц) =3H₃PO₄ + 5N⁺⁴O₂
3P + 5HNO₃ + 2H₂O =3H₃PO₄ + 5N⁺²O
С концентрированной серной кислотой образуется фосфорная кислота, оксид серы (+4) и вода
3P + 5H₂SO₄(конц.) =3H₃PO₄ + 5S⁺⁴O₂+ 2H₂O
4.ВЗАИМОДЕЙСТВИЕ С ЩЕЛОЧАМИ
С растворами щелочей образует фосфин и гипофосфит
4P⁰ + 3NaOH + 3H2O = P¯³H 3 + 3NaH 2 P ⁺1 O 2
5.ВЗАИМОДЕЙСТВИЕ С СОЛЯМИ
5.ВЗАИМОДЕЙСТВИЕ С СОЛЯМИ
С сильными окислителями, проявляя восстановительные свойства
3P⁰ + 5NaN⁺⁵O₃ = 5NaN⁺³O₂ + P₂⁺⁵O₅
ХИМИЧЕСКИЕ СВОЙСТВА УГЛЕРОДА
1.ВЗАИМОДЕЙСТВИЕ С МЕТАЛЛАМИ
реакции протекают при нагревании
Металлы – d-элементы образуют с углеродом соединения нестехиометрического состава типа твердых растворов: WC, ZnC, TiC – используются для получения сверхтвёрдых сталей
с углеродом карбиды 2Li + 2C = Li2C2,
Са + 2С = СаС2
2.ВЗАИМОДЕЙСТВИЕ С НЕМЕТАЛЛАМИ
Из галогенов непосредственно реагирует только с фтором, с остальными при нагревании.
С + 2F₂ = CF₄.
Взаимодействие с кислородом:
2С + О₂ (недост) = 2С⁺²О (угарный газ),
С + О₂(изб) = С⁺⁴О₂(углекислый газ).
Взаимодействие с другими неметаллами при повышенной температуре, не взаимодействует с фосфороМ
C + Si = SiC¯⁴ ; С + N₂ = C₂⁺⁴N₂ ;
C + 2H₂ = C¯⁴H₄ ; С + 2S = C⁺⁴S₂;
3.ВЗАИМОДЕЙСТВИЕ С ВОДОЙ
Пропускание водяных паров через раскаленный уголь – образуется угарный газ и водород (синтез-газ
C + H₂O = CO + H₂
4.ВЗАИМОДЕЙСТВИЕ С ОКСИДАМИ
УГЛЕРОД ВОССТАНАВЛИВАЕТ ПРИ НАГРЕВАНИИ МЕТАЛЛЫ И НЕМЕТАЛЛЫ ИЗ ОКСИДОВ ДО ПРОСТОГО ВЕЩЕСТВА (КАРБОТЕРМИЯ), в углекислом газе уменьшает степень окисления
2ZnO + C = 2Zn + CO; 4 С + Fe₃O₄ = 3Fe + 4CO ;
P₂O₅ + C = 2P + 5CO; 2 С + SiO₂ = Si + 2CO;
С + C⁺⁴O₂ = 2C⁺²O
5.ВЗАИМОДЕЙСТВИЕ С КИСЛОТАМИ
Окисляется концентрированными азотной и серной кислотой до углекислого газа
C +2H2SO4(конц)=C⁺⁴O2+ 2S⁺⁴O2+ 2H2O; C+4HNO3 (конц) =C⁺⁴O2 + 4N⁺⁴O2 + 2H2O.
С ЩЕЛОЧАМИ И СОЛЯМИ
НЕ РЕАГИРУЕТ
ХИМИЧЕСКИЕ СВОЙСТВА КРЕМНИЯ
1.ВЗАИМОДЕЙСТВИЕ С МЕТАЛЛАМИ
реакции протекают при нагревании: с кремнием реагируют активные металлы – силициды
4Cs + Si = Cs4Si,
1.ВЗАИМОДЕЙСТВИЕ С НЕМЕТАЛЛАМИ
Из галогенов непосредственно только с фтором.
С хлором реагирует при нагревании
Si + 2F2 = SiF4; Si + 2Cl2 = SiCl4;
Si + O₂ = SiO₂; Si + C = SiC; 3Si + 2N₂ = Si₃N;
С водородом не взаимодействует
3.ВЗАИМОДЕЙСТВИЕ С КИСЛОТАМИ
взаимодействует только со смесью плавиковой и азотной кислот, образуя гексафторокремниевую кислоту
3Si + 4HNO₃ + 18HF = 3H₂ + 4NO + 8H₂O
Взаимодействие с галогеноводородами (это не кислоты) – вытесняет водород, образуются галогениды кремния и водород
С фтороводородом реагирует при обычных условиях.
Si + 4HF = SiF₄ + 2H₂
4.ВЗАИМОДЕЙСТВИЕ С ЩЕЛОЧАМИ
Растворяется при нагревании в щелочах, образуя силикат и водород:
Si +2NaOH +H₂O = Na₂SiO₃ + 2H₂
Общая характеристика неметаллов.
Неметаллы ― химические элементы, которые образуют простые тела, не обладающие свойствами, характерными для металлов. Качественной характеристикой неметаллов является электроотрицательность.
Электроотрицательность ― это способность поляризовать химическую связь, оттягивать к себе общие электронные пары.
К неметаллам относят 22 элемента.
Положение неметаллических элементов в периодической системе химических элементов
1-й период | |||||||
2-й период | |||||||
3-й период | |||||||
4-й период | |||||||
5-й период | |||||||
6-й период |
Как видно из таблицы, неметаллические элементы в основном расположены в правой верхней части периодической системы.
Строение атомов неметаллов
Характерной особенностью неметаллов является большее (по сравнению с металлами) число электронов на внешнем энергетическом уровне их атомов. Это определяет их большую способность к присоединению дополнительных электронов и проявлению более высокой окислительной активности, чем у металлов. Особенно сильные окислительные свойства, т. е. способность присоединять электроны, проявляют неметаллы, находящиеся во 2-ом и 3-м периодах VI-VII групп. Если сравнить расположение электронов по орбиталям в атомах фтора, хлора и других галогенов, то можно судить и об их отличительных свойствах. У атома фтора свободных орбиталей нет. Поэтому атомы фтора могут проявить только валентность I и степень окисления ― 1. Самым сильным окислителем является фтор . В атомах других галогенов, например в атоме хлора, на том же энергетическом уровне имеются свободные d-орбитали. Благодаря этому распаривание электронов может произойти тремя разными путями. В первом случае хлор может проявить степень окисления +3 и образовать хлористую кислоту HClO 2 , которой соответствуют соли ― хлориты, например хлорит калия KClO 2 . Во втором случае хлор может образовать соединения, в которых степень окисления хлора +5. К таким соединениям относятся хлорноватая кислота HClO 3 и ее соли ― хлораты, например хлорат калия КClO 3 (бертолетова соль). В третьем случае хлор проявляет степень окисления +7, например в хлорной кислоте HClO 4 и в ее солях, ― перхлоратах (в перхлорате калия КClO 4).
Строения молекул неметаллов. Физические свойства неметаллов
В газообразном состоянии при комнатной температуре находятся:
водород ― H 2 ;
азот ― N 2 ;
кислород ― O 2 ;
фтор ― F 2 ;
хлор ― CI 2 .
И инертные газы:
гелий ― He;
неон ― Ne;
аргон ― Ar;
криптон ― Kr;
ксенон ― Xe;
радон ― Rn).
В жидком ― бром ― Br.
В твердом:
углерод ― C;
кремний ― Si;
фосфор ― P;
мышьяк ― As;
селен ― Se;
теллур ― Te;
астат ― At.
Гораздо богаче у неметаллов и спектр цветов: красный ― у фосфора, бурый ― у брома, желтый ― у серы, желто-зеленый ― у хлора, фиолетовый ― у паров йода и т. д.
Самые типичные неметаллы имеют молекулярное строение, а менее типичные ― немолекулярное. Этим и объясняется отличие их свойств.
Состав и свойства простых веществ - неметаллов
Неметаллы образуют как одноатомные, так и двухатомные молекулы. К одноатомным неметаллам относятся инертные газы, практически не реагирующие даже с самыми активными веществами. Инертные газы расположены в VIII группе периодической системы, а химические формулы соответствующих простых веществ следующие: He, Ne, Ar, Kr, Xe и Rn.
Некоторые неметаллы образуют двухатомные молекулы. Это H 2 , F 2 , Cl 2 , Br 2 , Cl 2 (элементы VII группы периодической системы), а также кислород O 2 и азот N 2 . Из трехатомных молекул состоит газ озон (O 3). Для веществ неметаллов, находящихся в твердом состоянии, составить химическую формулу довольно сложно. Атомы углерода в графите соединены друг с другом различным образом. Выделить отдельную молекулу в приведенных структурах затруднительно. При написании химических формул таких веществ, как и в случае с металлами, вводится допущение, что такие вещества состоят только из атомов. Химические формулы, при этом, записываются без индексов: C, Si, S и т. д. Такие простые вещества, как озон и кислород, имеющие одинаковый качественный состав (оба состоят из одного и того же элемента ― кислорода), но различающиеся по числу атомов в молекуле, имеют различные свойства. Так, кислород запаха не имеет, в то время как озон обладает резким запахом, который мы ощущаем во время грозы. Свойства твердых неметаллов, графита и алмаза, имеющих также одинаковый качественный состав, но разное строение, резко отличаются (графит хрупкий, алмаз твердый). Таким образом, свойства вещества определяются не только его качественным составом, но и тем, сколько атомов содержится в молекуле вещества и как они связаны между собой. Неметаллы в виде простых тел находятся в твердом или газообразном состоянии (исключая бром ― жидкость). Они не имеют физических свойств, присущих металлам. Твердые неметаллы не обладают характерным для металлов блеском, они обычно хрупки, плохо проводят электрический ток и тепло (за исключением графита). Кристаллический бор В (как и кристаллический кремний) обладает очень высокой температурой плавления (2075°С) и большой твердостью. Электрическая проводимость бора с повышением температуры сильно увеличивается, что дает возможность широко применять его в полупроводниковой технике. Добавка бора к стали и к сплавам алюминия, меди, никеля и др. улучшает их механические свойства. Бориды (соединения бора с некоторыми металлами, например с титаном: TiB, TiB 2) необходимы при изготовлении деталей реактивных двигателей, лопаток газовых турбин. Как видно из схемы 1, углерод ― С, кремний ― Si, бор ― В имеют сходное строение и обладают некоторыми общими свойствами. Как простые вещества они встречаются в двух видоизменениях ― в кристаллическом и аморфном. Кристаллические видоизменения этих элементов очень твердые, с высокими температурами плавления. Кристаллический кремний обладает полупроводниковыми свойствами. Все эти элементы образуют соединения с металлами ― карбиды, силициды и бориды (CaC 2 , Al 4 C 3 , Fe 3 C, Mg 2 Si, TiB, TiB 2). Некоторые из них обладают большей твердостью, например Fe 3 C, TiB. Карбид кальция используется для получения ацетилена.
Химические свойства неметаллов
В соответствии с численными значениями относительных электроотрицательностей окислительные способности неметаллов увеличивается в следующем порядке: Si, B, H, P, C, S, I, N, Cl, O, F.
Неметаллы как окислители
Окислительные свойства неметаллов проявляются при их взаимодействии:
с металлами: 2Na + Cl 2 = 2NaCl;
с водородом: H 2 + F 2 = 2HF;
с неметаллами, которые имеют более низкую электроотрицательность: 2Р + 5S = Р 2 S 5 ;
с некоторыми сложными веществами: 4NH 3 + 5O 2 = 4NO + 6H 2 O,
2FeCl 2 + Cl 2 = 2 FeCl 3 .
Неметаллы как восстановители
Все неметаллы (кроме фтора) проявляют восстановительные свойства при взаимодействии с кислородом:
S + O 2 = SO 2 , 2H 2 + O 2 = 2H 2 О.
Кислород в соединении с фтором может проявлять и положительную степень окисления, т. е. являться восстановителем. Все остальные неметаллы проявляют восстановительные свойства. Так, например, хлор непосредственно с кислородом не соединяется, но косвенным путем можно получить его оксиды (Cl 2 O, ClO 2 , Cl 2 O 2), в которых хлор проявляет положительную степень окисления. Азот при высокой температуре непосредственно соединяется с кислородом и проявляет восстановительные свойства. Еще легче с кислородом реагирует сера.
Многие неметаллы проявляют восстановительные свойства при взаимодействии со сложными веществами:
ZnO + C = Zn + CO, S + 6HNO 3 конц = H 2 SO 4 + 6NO 2 + 2H 2 О.
Существуют и такие реакции, в которых один и тот же неметалл является одновременно и окислителем и восстановителем:
Cl 2 + H 2 О = HCl + HClO.
Фтор ― самый типичный неметалл, которому нехарактерны восстановительные свойства, т. е. способность отдавать электроны в химических реакциях.
Соединения неметаллов
Неметаллы могут образовывать соединения с разными внутримолекулярными связями.
Виды соединений неметаллов

Общие формулы водородных соединений по группам периодической системы химических элементов приведены в таблицe:
Нелетучие водородные соединения | Летучие водородные соединения |
|||||
С металлами водород образует (за некоторым исключением) нелетучие соединения, которые являются твердыми веществами немолекулярного строения. Поэтому их температуры плавления сравнительно высоки. С неметаллами водород образует летучие соединения молекулярного строения (например, фтороводород HF, сероводород H 2 S, аммиак NH 3 , метан CH 4). В обычных условиях это газы или летучие жидкости. При растворении в воде водородные соединения галогенов, серы, селена и теллура образуют кислоты той же формулы, что и сами водородные соединения: HF, HCl, HBr, HI, H 2 S, H 2 Se, H 2 Te. При растворении в воде аммиака образуются аммиачная вода, обычно обозначаемая формулой NH 4 OH и называемая гидроксидом аммония. Ее также обозначают формулой NH 3 ∙H 2 O и называют гидратом аммиака.
С кислородом неметаллы образуют кислотные оксиды. В одних оксидах они проявляют максимальную степень окисления, равную номеру группы (например, SO 2 , N 2 O 5), а других ― более низкую (например, SO 2 , N 2 O 3). Кислотным оксидам соответствуют кислоты, причем из двух кислородных кислот одного неметалла сильнее та, в которой он проявляет более высокую степень окисления. Например, азотная кислота HNO 3 сильнее азотистой HNO 2 , а серная кислота H 2 SO 4 сильнее сернистой H 2 SO 3 .
Характеристики кислородных соединений неметаллов
Свойства высших оксидов (т. е. оксидов, в состав которых входит элемент данной группы с высшей степенью окисления) в периодах слева направо постепенно изменяются от основных к кислотным.
В группах сверху вниз кислотные свойства высших оксидов постепенно ослабевают. Об этом можно судить по свойствам кислот, соответствующих этим оксидам.
Возрастание кислотных свойств высших оксидов соответствующих элементов в периодах слева направо объясняется постепенным возрастанием положительного заряда ионов этих элементов.
В главных подгруппах периодической системы химических элементов в направлении сверху вниз кислотные свойства высших оксидов неметаллов уменьшаются.
Галогены.
Строение атомов галогенов
К галогенам относятся элементы VIII группы периодической системы, атомы этих элементов содержат на внешнем энергетическом уровне семь электронов и до его завершения им недостает только одного электрона, поэтому галогены проявляют яркие окислительные свойства. В подгруппе с увеличением порядкового номера эти свойства уменьшаются в связи с увеличением радиуса атомов: от фтора к астату ― и, соответственно, возрастают восстановительные свойства их. Аналогично уменьшается и значение относительной электроотрицательности галогенов. Как наиболее электроотрицательный элемент, фтор в соединениях с другими элементами проявляет постоянную степень окисления -1 . Остальные галогены могут проявлять как эту степень окисления в соединениях с металлами, водородом и менее электроотрицательными элементами, так и положительные нечетные степени окисления от +1 до +7 в соединениях с более электроотрицательными элементами: кислородом, фтором.
Простые вещества галогены и их свойства

Хлор, бром и йод в стеклянных сосудах
Характеризуя простые вещества ― галогены, необходимо вспомнить основные теоретические сведения о типах химической связи и кристаллическом строении вещества. В двухатомных молекулах галогенов атомы связаны ковалентной неполярной связью Г· ·Г или Г―Г и имеют молекулярную кристаллическую решетку.
При обычных условиях F 2 ― ярко-желтый, с оранжевым оттенком газ, Cl 2 ― желто-зеленый ядовитый газ с характерным удушливым запахом, Br 2 ― легколетучая бурая жидкость (пары брома сильно ядовиты, ожоги бромом очень болезненны и долго не заживают), а I 2 ― твердое кристаллическое вещество, способное к возгонке. В ряду F 2, Сl 2 , Br 2 , I 2 ― плотность простых веществ растет, а интенсивность окраски увеличивается. Следовательно, в изменении свойств атомов и простых веществ ― галогенов проявляется одинаковая закономерность: с увеличением порядкового номера неметаллические свойства ослабевают, а металлические ― усиливаются.
Химические свойства галогенов
Взаимодействие галогенов с металлами с образованием галогенидов:
2Na + I 2 ―― 2Na +1 I -1 (иодид натрия);
2Al + 3I 2 = 2Аl +3 I 3 -1 (иодид алюминия);
2Al + 3Br 2 = 2Al +3 Br 3 -1 (бромид алюминия).
При реакциях металлов побочных подгрупп (переходных металлов) с галогенами образуются галогениды с большой степенью окисления металла, например:
2Fe + 3Cl 2 = 2FеCl 3 ,
но 2НСl + Fe = FeCl 2 + Н 2 .
Взаимодействие галогенов с водородом с образованием галогеноводородов (тип связи ― ковалентная полярная, тип решетки ― молекулярная). Сравнение скорости химических реакций разных галогенов с водородом позволяет повторить зависимость ее от природы реагирующих веществ. Так, фтор имеет настолько большую скорость реакции, что взаимодействует с водородом с взрывом даже в темноте. Реакция хлора с водородом при обычных условиях идет медленно и лишь при поджигании или освещении скорость ее растет во много раз (происходит взрыв). Еще медленнее взаимодействуют с водородом бром и йод, причем последняя реакция приобретает уже эндотермический характер:

Только фтор взаимодействует с водородом необратимо, остальные галогены в зависимости от условий могут давать и обратимую реакцию.
Водные растворы галогеноводородов являются кислотами: HF ― фтороводородная (плавиковая), HCl ― хлороводородная (соляная), HBr ― бромоводородная, HI ― йодоводородная.
Галогены взаимодействуют с водой:
2F 2 + 2Н 2 O = 4HF + O 2
Вода во фторе горит, кислород является не причиной, а следствием горения, выступая в непривычной для него роли восстановителя.
Для характеристики способности одних галогенов (не атомов галогенов, а простых веществ) к вытеснению других из растворов их соединений можно использовать «ряд активности» галогенов, который записывается так:
F 2 > Сl 2 > Вr 2 > I 2 ,
т. е. окислительные свойства уменьшаются.
Так, хлор вытесняет бром и йод (но не фтор), а бром в состоянии вытеснить только йод из растворов соответствующих солей:
2NaBr + Cl 2 = 2NаСl + Br 2
2КI + Br 2 = 2КВr + I 2 .
Биологическое значение и применение галогенов
Фтор играет очень важную роль в жизни растений, животных и человека. Без фтора невозможно развитие костного скелета и особенно зубов. Содержание фтора в костях составляет 80-100 мг на 100 г сухого вещества. В эмали фтор присутствует в виде соединения Ca 4 F 2 (PO 4) 2 и придает ей твердость и белизну. При недостатке фтора в организме человека происходит поражение зубной ткани (кариес), а избыток его способствует заболеванию зубов флюорозом. Суточная потребность человека во фторе – 2-3 мг. Хлор (хлор-ион) более важен для жизнедеятельности животных и человека, чем для растений. Он входит в состав почек, легких, селезенки, крови, слюны, хрящей, волос. Ионы хлора регулируют буферную систему крови. Хлорид натрия является составной частью плазмы крови и спинномозговой жидкости и участвует в регуляции водного обмена в организме. Свободная соляная кислота входит в состав желудочного сока всех млекопитающих и активно участвует в пищеварении. У здорового человека содержится в желудке 0,2-0,3% соляной кислоты. Недостаток хлора в организме приводит к тахикардии, снижению артериального давления, судорогам. Достаточное количество хлора содержится в таких овощах как сельдерей, редис, огурцы, капуста белокочанная, укроп, перец, лук, артишок. Бром также входит в число необходимых микроэлементов и больше всего его содержится в гипофизе, крови. Щитовидной железе, надпочечниках. Бромиды в небольших дозах (0,1-0,3 взрослого человека) положительно действуют не центральную нервную систему как усилители процессов торможения в коре головного мозга. В природе бромиды накапливаются в таких растениях, как рожь, пшеница, ячмень, картофель, морковь, черешня, яблоки. Много брома содержится в голландском сыре. Йод в организме человека начинает накапливаться еще в утробе матери. В гормоне щитовидной железы человека ― тироксине ― содержится 60% связанного йода. Этот гормон с током крови поступает в печень, почки, молочные железы, желудочно-кишечный тракт. Недостаток йода в организме человека вызывает такие заболевания, как эндемический зоб и кретинизм, при котором замедляется рост и развивается умственная отсталость. В сочетании с другими элементами йод способствует росту и упитанности животных, улучшает их здоровье и плодовитость. Основными поставщиками йода для человека служат злаки, баклажаны, фасоль, капуста белокочанная и цветная, картофель, лук, морковь, огурцы, тыква, салат, морская капуста, кальмары.
Государственный образовательный стандартВводится с момента утверждения Москва 2000 г. Общая характеристика направления подготовки дипломированного специалиста “Безопасность... , типы взаимодействия, сплавы, применение в технике. Неметаллы , свойства, применение, важнейшие соединения – оксиды...
Раздел 6 содержание образования начальное общее образование
ДокументВ природе. 3. Царство грибы (3 ч) Грибы. Общая характеристика грибов, их строение и жизнедеятельность. Дрожжи... распознавание и получение веществ. ТЕМА 2 Неметаллы (27 час.) Общая характеристика неметаллов : положение в периодической системе Д. И. ...
Основная образовательная программа начального основного и среднего общего образования « средняя общеобразовательная школа № 10»
Основная образовательная программаКонкретизируются общие цели основного общего образования с учётом специфики учебного предмета; 2) общую характеристику учебного... в растворах электролитов. Многообразие веществ Общая характеристика неметаллов на основе их положения в периодической...
Лекция 24
Неметаллы.
План лекции:
Неметаллы – простые вещества
Положение неметаллов в периодической системе
Число элементов-неметаллов значительно меньше, чем элементов-металлов Типичными неметаллическими свойствами обладают десять химических элементов (Н, С, N, Р, О, S, F, Cl, Br, I). Шесть элементов, которые обычно относят к неметаллам, проявляют двойственные (и металлические, и неметаллические) свойства (В, Si, As, Se, Те, At). И еще 6 элементов в последнее время стали включать в список неметаллов. Это так называемые благородные (или инертные) газы (Не, Ne, Аг, Кг, Хе, Rn). Итак, 22 из известных химических элементов принято относить к неметаллам.
Элементы, проявляющие неметаллические свойства в периодической системе располагаются выше диагонали бор-астат (рис. 26).
Атомы большинства неметаллов, в отличие от атомов металлов, на внешнем электронном слое имеют большое число электронов - от 4 до 8. Исключение составляют атомы водорода, гелия, бора, которые имеют на внешнем уровне 1, 2 и 3 электрона соответственно.
Среди неметаллов только два элемента - водород (1s 1) и гелий (1s 2) относятся к s-семейству, все остальные принадлежат к р -семейству.
Атомы типичных неметаллов (A) характеризуются высокой электроотрицательностью и большим сродством к электрону, что обусловливает их способность образовывать отрицательно заряженные ионы с электронными конфигурациями соответствующих инертных газов:
А 0 + nê → А n -
Эти ионы входят в состав ионных соединений неметаллов с типичными металлами. Отрицательные степени окисления неметаллы имеют также в ковалентных соединениях с другими менее электроотрицательными неметаллами (в частности, с водородом).
Атомы неметаллов в ковалентных соединениях с более электроотрицательными неметаллами (в частности, с кислородом) имеют положительные степени окисления. Высшая положительная степень окисления неметалла , как правило, равна номеру группы , в которой он находится.
Неметаллы – простые вещества
Несмотря на небольшое число элементов-неметаллов, их роль и значение как на Земле, так и в космосе огромны. 99% массы Солнца и других звезд составляют неметаллы водород и гелий. Воздушная оболочка Земли состоит из атомов неметаллов - азота, кислорода и благородных газов. Гидросфера Земли образована одним из важнейших для жизни веществ - водой, молекулы которой состоят из неметаллов водорода и кислорода. В живой материи главенствуют 6 неметаллов - углерод, кислород, водород, азот, фосфор, сера.
При обычных условиях вещества-неметаллы существуют в разных агрегатных состояниях:
1) газы: водород Н 2 , кислород О 2 , азот N 2 , фтор F 2 , хлор С1 2 , инертные газы: Не, Ne, Ar, Кг, Хе, Rn
2) жидкости: бром Вг 2
3) твердые вещества йод I 2 , углерод С, кремний Si, сера S, фосфор Р и др.
Семь элементов-неметаллов образуют простые вещества, существующие в виде двухатомных молекул Э 2 (водород Н 2 , кислород О 2 , азот N 2, фтор F 2 , хлор С1 2 , бром Вг 2, йод I 2) .
Так как в кристаллической решетке неметаллов между атомами нет свободных электронов, они отличаются по физическим свойствам от металлов:
¾ не имеют блеска;
¾ хрупкие, имеют различную твердость;
¾ плохо проводят тепло и электричество.
Твердые вещества-неметаллы в воде практически нерастворимы; газообразные О 2 , N 2 , Н 2 и галогены обладают очень малой растворимостью в воде.
Для ряда неметаллов характерна аллотропия - явление существование одного элемента в виде нескольких простых веществ. Аллотропные модификации известны для кислорода (кислород О 2 и озон О 3), серы (ромбическая, моноклинная и пластическая), фосфора (белый, красный и черный), углерода (графит, алмаз и карбин и др.), кремния (кристаллический и аморфный).
Химические свойства неметаллов
По химической активности неметаллы существенно различаются между собой. Так, азот и благородные газы, в химические реакции вступают только при очень жестких условиях (высокое давление и температура, наличие катализатора).
Наиболее химически активными неметаллами являются галогены, водород и кислород. Сера, фосфор, а особенно углерод и кремний реакционноспособны только при повышенных температурах.
Неметаллы в химических реакциях проявляют и окислительные, и восстановительные свойства. Наиболее высокая окислительная способность характерна для галогенов и кислорода. У таких неметаллов, как водород, углерод, кремний, преобладают восстановительные свойства.
I. Окислительные свойства неметаллов:
1. Взаимодействие с металлами. При этом образуются бинарные соединения: с кислородом – оксиды, с водородом – гидриды, азотом – нитриды, галогенами – галогениды и т.д.:
2Cu + O 2 → 2CuO
2Fe + 3Cl 2 → 2FeCl 3
2. Взаимодействие с водородом. Неметаллы выступают в качестве окислителей и в реакциях с водородом, образуя при этом летучие водородные соединения:
Н 2 + С1 2 → 2НС1
N 2 + 3Н 2 → t, p, кат. 2NH 3
3. Взаимодействие с неметаллами. Неметаллы проявляют окислительные свойства также в реакциях с менее электроотрицательными неметаллами:
2Р + 5С1 2 → 2РС1 5 ;
С + 2S → CS 2 .
4. Взаимодействие со сложными веществами. Окислительные свойства неметаллов могут проявляться и в реакциях со сложными веществами. Например, вода горит в атмосфере фтора:
2F 2 + 2Н 2 О → 4HF + О 2 .
II. Восстановительные свойства неметаллов
1. Взаимодействие с неметаллами . Восстановительные свойства неметаллы могут проявлять по отношению к неметаллам с большей электроотрицательностью, и в первую очередь по отношению к фтору и кислороду:
4Р + 5О 2 → 2Р 2 О 5 ;
N 2 + О 2 → 2NO
2. Взаимодействие со сложными веществами. Некоторые неметаллы могут являться восстановителями, что позволяет применять их в металлургическом производстве:
С + ZnO → Zn + СО;
5Н 2 + V 2 О 5 → 2V + 5Н 2 О.
SiО 2 + 2С → Si + 2СО.
Восстановительные свойства неметаллы проявляют при взаимодействии со сложными веществами - сильными окислителями, например:
3S + 2КСlO 3 → 3SO 2 + 2КС1;
6Р + 5КСlO 3 → ЗР 2 O 5 + 5КС1.
С + 2H 2 SО 4 → СО 2 + 2SО 2 + 2Н 2 О;
3Р + 5HNО 3 + 2Н 2 О → ЗН 3 РО 4 + 5NO.
Общие способы получения неметаллов
Некоторые неметаллы встречаются в природе в свободном состоянии: это сера, кислород, азот, благородные газы. В первую очередь простые вещества - неметаллы входят в состав воздуха.
Большие количества газообразных кислорода и азота получают ректификацией воздуха (разделением).
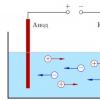
Наиболее активные неметаллы - галогены - получают электролизом расплавов или растворов из соединений. В промышленности с помощью электролиза в больших количествах получают одновременно три важнейших продукта: ближайший аналог фтора - хлор, водород и гидроксид натрия. В качестве электролита используют раствор хлорида натрия, подаваемый в электролизер сверху.
Более подробно способы получения неметаллов будут рассмотрены далее, в соответствующих лекциях.
Все известные на сегодняшний день химические элементы имеют общий "дом" - периодическую систему. Однако располагаются они там не как придется, а в строгом порядке, определенной последовательности. Одним из главных критериев, по которым классифицируются все атомы, являются характеристики.
Неметаллов и представителей металлических элементов - это основа, на которой базируется не только их разделение в пределах таблицы, но и области применения человеком. Познакомимся ближе с неметаллами и их характеристикой.
Положение в периодической системе
Если рассмотреть систему химических элементов в целом, то можно определить место положения неметаллов так:
- Верхний правый угол.
- Выше условной граничной диагонали от бора до астата.
- Главные подгруппы с IV-VIII группу.
Очевидно, что количество их явно уступает таковому у металлов. По численному соотношению это будет примерно 25/85. Однако данный факт нисколько не уменьшает их значимости и важности. При этом физические свойства неметаллов гораздо более разнообразные, чем таковые у их "оппонентов".
Разновидности простых соединений неметаллов
Определяют несколько основных категорий, к которым относятся все известные рассматриваемые элементы. Физические свойства - неметаллов - позволяют разделить их на:
- твердые;
- газообразные;
- жидкие.
При этом есть и особая группа элементов - благородные газы. По своим характеристикам они не относятся ни к одной из обозначенных категорий.

Газообразные неметаллы
Таковых достаточно много. К ним относятся такие простые вещества, как:
- кислород;
- азот;
- галогены хлор и фтор;
- водород;
- белый фосфор;
- озон.
Однако такое возможно при условии стандартных параметров окружающей среды. Кристаллическая решетка этих представителей - молекулярная, тип химической связи в молекулах - ковалентная неполярная. Физические свойства группы схожи. Они обладают:
- сжимаемостью;
- способностью безграничного смешения между собой;
- расширяемостью;
- заполняют весь объем сосуда.
Среди приведенных веществ ядовитыми являются два - хлор и Очень опасные, удушающие соединения. При этом хлор - желто-зеленый газ, фосфор - белый, легко воспламеняющийся на воздухе.
Кислород и озон - хорошие окислители. Первый - постоянный компонент воздуха, необходимый для жизни большинства организмов. Второй образуется после грозы при действии электрических разрядов молнии на кислород воздуха. Имеет приятный запах свежести.

Жидкие неметаллы
Физические свойства неметаллов этой группы можно описать, дав характеристику всего лишь одному веществу - брому. Поскольку только он является жидкостью при обычных условиях среди всех представителей рассматриваемой группы элементов.
Это темно-бурая жидкость, достаточно тяжелая, которая является сильнейшим ядом. Даже пары брома способны вызывать сложные, не заживающие долгое время язвы на руках. Запах его очень неприятный, за что элемент и получил свое название (в переводе bromos - зловонный).

По своим химическим характеристикам бром является окислителем для металлов и восстановителем для более сильных неметаллов, чем он сам.
Несмотря на такие особенности, ионы брома обязательно должны присутствовать в организме человека. Без него возникают заболевания, связанные с гормональными нарушениями.
Твердые представители
К простым веществам этой категории относится большинство неметаллов. Это:
- все углерода;
- красный и черный фосфор;
- сера;
- кремний;
- мышьяк;
- одна из модификаций олова.
Все они имеют достаточно твердые, но хрупкие вещества. Черный фосфор - жирное на ощупь сухое соединение. Красный же - пастообразная масса.

Самым твердым из всех обозначенных веществ является алмаз - разновидность углерода. Физические и химические свойства неметаллов данной группы очень разные, так как в таблице располагаются некоторые из них далеко друг от друга. Значит, степени окисления, проявляемая химическая активность, характер соединений - все эти показатели будут варьироваться.
Интересным неметаллом в твердом состоянии является йод. Его кристаллы блестят на срезе, проявляя тем самым схожесть с металлами. Это не удивительно, ведь он располагается практически на границе с ними. Также есть у этого вещества особое свойство - сублимация. При нагревании йод переходит в газообразное состояние, минуя жидкое. Пары его имеют ярко-фиолетовую насыщенную окраску.
Физические свойства неметаллов: таблица
Чтобы проще обозначить, что собой представляют неметаллы, лучше выстроить обобщающую таблицу. Она покажет, в чем заключаются общие физические свойства неметаллов, а в чем проявляются их различия.
| Физическое свойство | Пример неметалла |
| при обычных условиях | Характерны все три: твердое (сера, углерод, кремний и прочие), газообразное (например, галогены), жидкое (бром) |
| Электро- и теплопроводность | Не характерна ни для чего, кроме углерода и черного фосфора |
| Окраска простого вещества | Очень разнообразная. Пример: бром - красный, сера - желтая, кристаллы йода - темно-фиолетовые, углерод в виде графита - темно-серый, хлор - желто-зеленый и так далее |
| Металлический блеск | Характерен только для кристаллического йода |
| Ковкость и пластичность | Полностью отсутствует. Все твердые вещества - хрупкие, кроме алмаза и некоторых форм кремния |
Очевидно, что в физических свойствах неметаллов больше преобладают различия, нежели сходства. Если для металлов можно выделить несколько характеристик, под которые будет подпадать каждый из них, то для рассмотренных нами элементов такое невозможно.
Неметаллы — элементы с 14-ой по 16-ую группы таблицы Менделеева . Они почти не проводят электричество и тепло. Неметаллы очень хрупкие и практически не изгибанию и любым другим деформациям. Они могут существовать в 2х из 3х состояний материи при комнатной температуре: газ (например, кислород) и твердые вещества (например, углерод). Неметаллы, не обладают металлическим блеском и не отражают свет.
Взаимодействие неметаллов с простыми веществами.
1. Взаимодействие неметаллов с металлами :
2Na + Cl 2 = 2NaCl ,
Fe + S = FeS ,
6Li + N 2 = 2Li 3 N ,
2Ca + O 2 = 2CaO.
в подобных случаях неметаллы проявляют окислительные свойства (принимают электроны, образуя отрицательно заряженные частицы).
2. Взаимодействие неметаллов с другими неметаллами:
- взаимодействуя с водородом, почти все неметаллы проявляет окислительные свойства, при этом образуя летучие водородные соединения - ковалентные гидриды:
3H 2 + N 2 = 2NH 3 ,
H 2 + Br 2 = 2HBr ;
- взаимодействуя с кислородом, все неметаллы, кроме фтора , проявляют восстановительные свойства:
S + O 2 = SO 2 ,
4P + 5O 2 = 2P 2 O 5 ;
- при взаимодействии с фтором фтор является окислителем, а кислород - восстановителем:
2F 2 + O 2 = 2OF 2 ;
- неметаллы взаимодействуют между собой, более электроотрицательный металл играет роль окислителя, менее электроотрицательный - роль восстановителя:
S + 3F 2 = SF 6 ,